Inhaltsverzeichnis
Reagenzglas ohne Etikett
Vorhanden sind elf Chemikalien. Dabei kann es sich um n-Butanol, Harnstoff, Oxalsäure, Glucose, Propansäure, n-Heptan, Glycerin, Cyclohexen, Isobutanol, Dodecanol, Cetylalkohol und Palmitinsäure handeln.
Aufgabe: Einen (möglichst einfachen) Versuchsplan zu entwicklen, durchzuführen und zu protokollieren, durch den die Stoffe mit den Nummern (1) bis (11) benannt werden können.
Als Hilfe stehen Informationskärtchen1), das Schulbuch, ein Chemie-Lexikon sowie Hilfekarten für das Verfahrensschema und das Auswerteraster zur Verfügung.
Benötigte Eigenschaften
| Stoff | Schmelztemperatur | Löslich in Wasser | pH | Dichte | Reaktion mit Bromwasser | Stoffprobe |
|---|---|---|---|---|---|---|
| n-Butanol | -90 °C | kaum | 0,831 g/ml | 1 | ||
| Harnstoff | 133 °C | gut | = 7 | 2 | ||
| Oxalsäure | 102 °C | gut | < 7 | 3 | ||
| Glucose | 85 °C | gut | = 7 | 4 | ||
| Propansäure | -22 °C | gut | < 7 | 5 | ||
| n-Heptan | -91 °C | nicht | 0,681 g/ml | 6 | ||
| Glycerin | 18 °C | gut | = 7 | 7 | ||
| Cyclohexen | -80 °C | nicht | ja | 8 | ||
| Isobutanol | -108 °C | mäßig | 11 | |||
| Dodecanol | 24 °C | nicht | fehlt | |||
| Cetylalkohol | 49 °C | nicht | 9 | |||
| Palmitinsäure | 63 °C | nicht | 10 |
Ergebnis

Isobutanol und n-Butanol ließen sich über die Wasserlöslichkeit nur schwer unterscheiden, daher wird überlegt, im Wiederholungsfall nur einen der beiden Stoffe einzusetzen. Auch wäre die Recherche am PC wahrscheinlich noch als zusätzliche Hilfe günstig.
Analyse durch Reaktionen
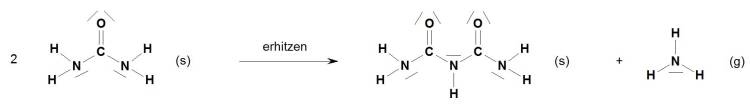
- Erhitzen
- Glucose (Verbrennung bzw. Oxidation, Karamell ist ein Zwischenprodukt): C6H12O6 (s) + O2 (g) → 6 CO2 (g) + 6 H2O (g)
- Reaktion mit Bromwasser: siehe Reaktionsmechanismus: Elektrophile Addition
Visualisierung der Moleküle
:!:Da Jmol erst zu Jsmol aktualisiert werden muss, funktioniert die Moleküldarstellung zur Zeit nicht.
|
Glucose <jmol glucose.mol></jmol> |
Harnstoff <jmol harnstoff.mol></jmol> |
Biuret <jmol biuret-molekuel.mol></jmol> |
- Klick mit der linken Maustaste auf die Abbildungen, Maus bewegen: Das Molkül lässt sich drehen.
- Klick mit rechter Maustaste auf die Abbildungen: öffnet ein Menü mit Einstellmöglichkeiten, z.B.
- Surfaces > Dot Surface : Erzeugt die van-der-Waals-Oberfläche in Pünktchen-Form
- Style > Schema >
- CPK Spacefill : Kalottenmodell
- Drahtgitter: Stäbchenmodell
Herumspielen und Ausprobieren erlaubt und erwünscht. 
— Jmol: an open-source Java viewer for chemical structures in 3D. http://www.jmol.org/
— Berechnungen mit Avogadro: an open-source molecular builder and visualization tool. Version 1.0.3 http://avogadro.openmolecules.net/